TANAKA TOMOHITO
医学部 産婦人科学教室
総合医学研究センター
トランスレーショナルリサーチ部門(TR部門)
教授
研究開発段階
研究のポイント
- あらゆる腫瘍のPDXを作成、解析しており、即時利用可能
- 腫瘍本体、PDX、生体サンプルをバイオバンクに保存してある
- ターゲットとしたい遺伝子異常、タンパク増幅のあるPDXで実験できる
研究キーワード
卵巣癌、子宮頸癌、子宮体癌、PDX、細胞外小胞
研究の背景
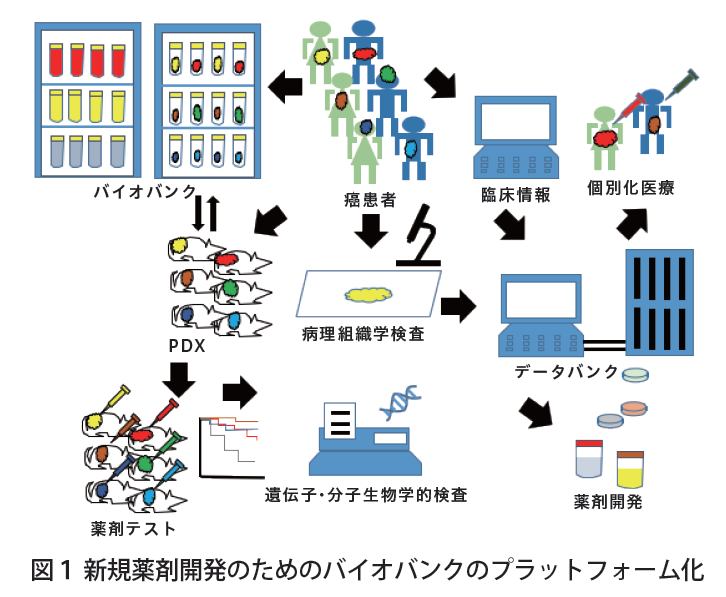
これまでは、薬剤開発の実験には細胞株が用いられてきた。細胞株は同一の遺伝情報をもつため、その再現性や実験のしやすさなどの利点がある半面、多様性に欠け、生体内での薬剤感受性を反映しないなどの問題があげられている。臨床腫瘍直接移植モデル(PDX)は腫瘍片をマウスに直接移植し、より原発腫瘍に近いモデルとして注目されている。
そこで、PDX を作成し、腫瘍本体、PDX および、術前・術後の血液や体腔液などの生体サンプルをバイオバンクで保存するとともに、臨床情報のみならず、シーケンサーなどで解析したDNA・RNA・蛋白などの情報や、薬剤感受性をデータとして蓄積し、新規薬剤開発を行うためのデータバンクの構築を目指している。(図1)
現在、このプラットフォームを用いて、バイオマーカーとしての細胞外小胞の解析、新規核酸治療薬の開発、ホウ素中性子捕捉療法(BNCT)の研究が進められている。
研究の概要・進行状況
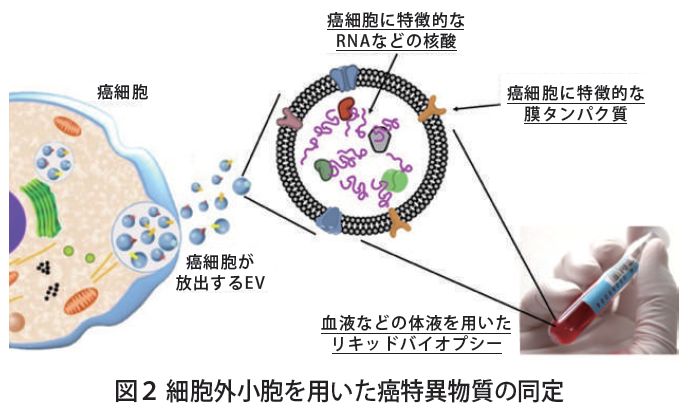
バイオバンクに保存してあるサンプルを即時利用することが可能であり、腫瘍本体、術前・術後の血液、体腔液などから、早期発見マーカーや、薬剤感受性の指標となるバイオマーカーを解析することができる。実際に、卵巣癌症例で、術前・術後の血液中細胞外小胞を比較することにより、卵巣明細胞癌に特異的なマイクロRNA を同定し、早期発見マーカーとしての解析を進めている。さらに、卵巣癌治療のキードラックであるプラチナ製剤感受性に関与する細胞外小胞内のRNA 修飾体を同定し、プラチナ製剤投与前にその感受性を判定する検査方法として特許出願中である。(図2)
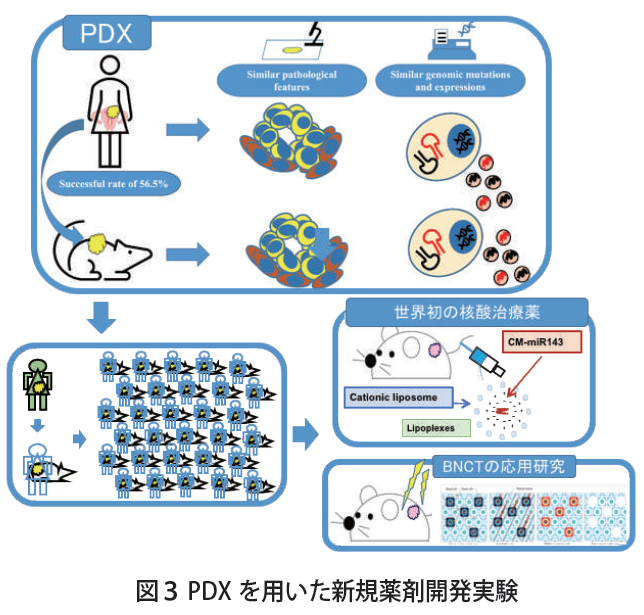
PDXでは、子宮頸癌、子宮体癌での生着率は約50%で、原発腫瘍の病理組織学的な特徴を反映し、同様のDNA変異やRNA発現、タンパク発現を有していることを証明してある。さらに、放出される細胞外小胞も類似していることを確認してある。また、腹水、胸水などの体腔液からのPDX作成にも成功しており、新規薬剤のターゲットとなる遺伝子異常やタンパク増幅あるいは特定の表面抗原を有している腫瘍などに合致するPDXがあれば、複製し実験に用いることができる。現在、子宮癌PDXを用いて、新規核酸治療薬の開発、BNCTの研究が進められている。(図3)
市場性
2024年度時点で保有するサンプル合計は35種類の腫瘍について250点である。
想定する社会実装の形
バイオマーカーに関しては、簡便な検査キットとして実装し、検査項目(保険適用)として扱う予定である。
PDXに関しては組織診断の際の検査項目とすることを検討している。
連携先へのメッセージ
社会実装に向けた研究を推進するため、新規薬剤開発を行っている研究者や企業との共同研究を求めています。
関連論文・知財
- Creation and Validation of Patient-Derived Cancer Model Using Peritoneal and Pleural Effusion in Patients with Advanced Ovarian Cancer: An Early Experience. Nishie R, Tanaka T, et al. J Clin Med 13(9), 2718, 2024
- Consistency between Primary Uterine Corpus Malignancies and Their Corresponding Patient-Derived Xenograft Models. Ued S , Tanaka T, et al. Int J Mol Sci. 25(3), 1486, 2024
- Cancer-Specific miRNAs Extracted from Tissue-Exudative Extracellular Vesicles in Ovarian Clear Cell Carcinoma. Maruoka H, Tanaka T, et al. Int J Mol Sci. 23(24), 15715, 2022
[特許]出願中