JIN DENAN
医学部 薬理学教室
准教授
研究開発段階
研究のポイント
- 肥満細胞由来のキマーゼの活性化とPTFE人工血管内膜肥厚形成との関連性
- 内膜肥厚形成に対するキマーゼ阻害薬コーテイン人工血管の抑制効果の検証
- キマーゼ阻害薬コーテインPTFE人工血管の臨床応用への試み
研究キーワード
腎透析、PTFE人工血管、バスキュラーアクセス不全、キマーゼ阻害薬、コーティング
研究の背景
近年、腎透析レベルの向上によって末期腎不全患者のライフスパンが十数年から数十年も延長されている。透析患者は週3回血液透析を行わなければならない。短時間の透析で効率よく血液を浄化するには穿刺しやすく、かつ血流量の豊富な血管の確保が不可欠である。そこで、透析患者には通常動静脈シャント術(内シャント)あるいは動静脈間PTFE人工血管移植術(人工血管グラフト)が施される(図1)。しかし、このように作製されたバスキュラーアクセスのいずれも、その後の血管内膜肥厚による内腔狭窄によって充分な血液量が確保できず、新たなバスキュラーアクセスルートの作製が強いられるようになる。近年、本邦におけるこのような再建術に使われる医療費が年々上昇し、医療保険制度に多大な負担をかけているだけではなく、患者における肉体的と経済的な損失も非常に大きい。しかし、バスキュラーアクセス不全に対する有効な治療法などが未だに開発されていないのが現状である。
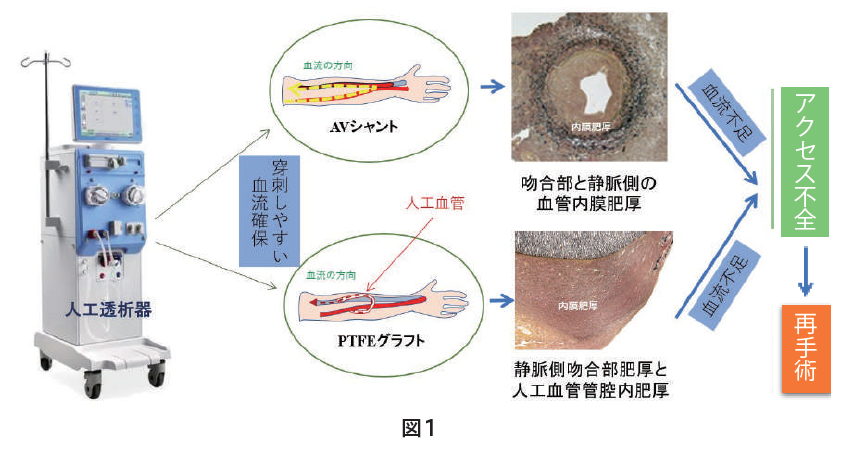
研究の概要・進行状況
キマーゼは肥満細胞内に貯蔵されている酵素の一つであり、アンジオテンシン変換酵素と同様にアンジオテンシン(Ang)IをAngIIへと変換可能だけではなく、TGFβ1やMMPsなどの活性化にも寄与している。我々はこれまでに、イヌの内シャントやPTFE人工血管移植モデルを作製し、キマーゼ阻害薬の血管内膜肥厚に対する効果を検討してきた(関連論文1-3)。結果、キマーゼ阻害薬の長期経口投与は血管内膜肥厚の形成を有意に抑制し、キマーゼ阻害薬の透析患者のバスキュラーアクセス不全に対する予防薬になる可能性を指摘してきた。また、これらの研究を介して、PTFE人工血管移植後にみられる線維芽細胞の外膜側からの管腔内への遊走機構がその内膜肥厚形成に非常に重要であることも突き止めた。そこで、我々はキマーゼ阻害薬のPTFE人工血管へのコーティングがこのような線維芽細胞の遊走を抑えられないのではないかと考え、関西大学との共同研究によってキマーゼ阻害薬をPTFE人工血管へコーティングすることができた。キマーゼ阻害薬コーティングと非コーティングPTFE人工血管を10匹のイヌにそれぞれ移植した結果、キマーゼ阻害薬のコーティング群の移植6カ月後の内膜肥厚形成が有意に抑制されることが明らかとなった(図2)。
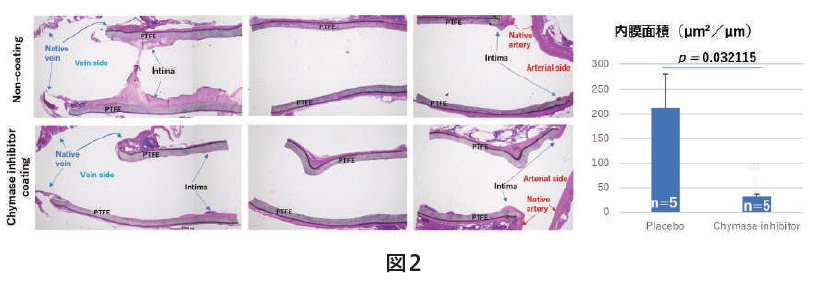
市場性
2022年末の施設調査結果によると、本邦における透析患者数は347,474人であり、人口百万人あたりの患者数は2,781人である。その中で、89.7%の透析の患者は内シャントというバスキュラーアクセスルートによって管理されており、体表血管に乏しい症例や動脈閉塞症などの症例ではPTFE人工血管移植術によるバスキュラーアクセスルートが透析管理に用いられており、その割合はおよそ7.1%であった。この割合は海外の使用例よりかなり少ないとされている。通常、内シャントによるバスキュラーアクセスの開存期間がより長く、透析患者に優先されるべきであるが、やむを得ず、PTFE人工血管移植術を受けられた場合、その開存期間が非常に短いのが特徴である。人工血管を用いたバスキュラーアクセスルートのおよそ50%は1年以内に管腔内狭窄に見舞われ、血流量低下によるバスキュラーアクセス不全に陥ってしまう。そして、委嘱2年後の開存率はわずか10%以下であり、新たなバスキュラーアクセスルートを作製しなければならなくなる。このようなアクセスルートの作製に必要な費用全額が約30万円であり、自己負担が3割の場合は約9万円である。
想定する社会実装の形
現在、PTFE人工血管を腎透析患者のバスキュラーアクセスルートとして使用されている割合は年々増加する傾向にあり、バスキュラーアクセス不全のために行う再手術の回数も増えつつあり、患者と医療保険制度に大きな負担をかけている。我々の研究で示しているように、キマーゼ阻害薬コーティングPTFE人工血管はイヌへの頚動静脈間移植6カ月後の血管内膜肥厚形成を非コーティング群に比べて大きく抑制しており、キマーゼ阻害薬コーティング技術の臨床応用が現在腎透析患者のPTFE人工血管バスキュラーアクセスの開存期間を大きく延長できる可能性を伺わせている。
また、我々がこれまでのキマーゼ阻害薬の経口投与効果を検討した研究では、キマーゼ阻害薬の投与はPTFE人工血管内腔の内膜肥厚形成だけではなく、肥厚部位における血栓付着も非投薬群に比べて有意に抑制しており、PTFE人工血管の血栓易形成性といったデメリットも克服できるのではないかと期待をかけている。このように、現在臨床で主に使われているPTFE人工血管のバスキュラーアクセスの使用可能な期間はキマーゼ阻害薬のコーティングによって大きく延長されることが予想され、患者の経済的な負担軽減だけではなく、年々膨らむ医療保険の抑制対策にもつながると考えている。
連携先へのメッセージ
日本には非常に優れた医療用デバイスメーカーが数多く存在し、各種研究費助成制度も充実しています。我々の研究結果を臨床へつなげていくには産学官の連携が不可欠であり、今後、興味のあるメーカーとの共同研究と科研費獲得に尽力していくつもりです。
また、現在日本と海外で透析に主に使用されている人工血管はPTFE素材からなっており、この素材自体の隙間構造に内膜肥厚形成機序が潜んでいます。PTFE人工血管移植後にこのような隙間から外膜側の線維芽細胞が管腔内へ遊走し、その管腔内内膜肥厚に大きく寄与していることを我々が見出してきました。そこで、我々は人工血管移植後の管腔内内膜肥厚形成を防ぐにはPTFEのような隙間構造を持たない新たな生体適合性素材からなる人工血管の開発も不可欠ではないかとも考えています。これまでに、我々は中層無孔体からなる人工血管を用いて内膜肥厚形成におけるPTFE人工血管との差異についてイヌの移植モデルで比較検討を行ってみましたが、やはり、移植後の線維芽細胞の管腔内遊走を抑制可能な中層無孔体人工血管の方が内膜肥厚形成を非常に有効的に抑えることが明らかとなりました(関連論文3)。しかし、この中層無孔体の人工血管は結構固く、移植術にあまり向いてない理由で販売中止となりました。現在、PTFE人工血管は世界的にアメリカの会社がほぼ独占販売しており、もし内膜肥厚形成を有効的に抑制できる新たな人工血管が開発されれば、PTFE人工血管の独占市場を揺るがすものになるのではないかと考えています。
関連論文・知財
- Effect of chymase inhibition on the arteriovenous fistula stenosis in dogs. Jin D, Ueda H, Takai S, Okamoto Y, Muramatsu M, Sakaguchi M, Shibahara N, Katsuoka Y, Miyazaki M. J Am Soc Nephrol 16, 1024-1034, 2005
- Roles of chymase in stenosis occurring after polytetrafluoroethylene graft implantations. Jin D, Ueda H, Takai S, Muramatsu M, Furubayashi K, Ibaraki T, Kishi K, Katsuoka Y, Miyazaki M. Life Sci 29(81), 1291-1300, 2007
- Outside fibroblasts play a key role in the development of inn er neointima after the implantation of polytetrafluoroethylene grafts. Jin D, Takai S, Li Z, Sakonjo H, Otsuki Y, Shibayama Y, Miyazaki M. J Pharmacol Sci 119, 139-49, 2012
[特許]出願中