研究テーマ
“遺伝子解析から丸ごとの動物実験”により病態の解明と治療薬の開発を目指す
腎疾患(急性腎障害や慢性腎臓病など)や心血管疾患の発症には様々な生体内因子が関与しています。我々の研究室では、血管収縮物質としては最も強力なエンドセリンと呼ばれるペプチドや極めて重要な血管弛緩物質である一酸化窒素などの生理活性物質、さらには血管拡張に関与する可溶性グアニル酸シクラーゼにフォーカスをあて、種々の病態モデル動物を用いて、各種循環器疾患との関わりについて検討しています。
キーワード
急性腎障害、慢性腎臓病、虚血性臓器障害、可溶性グアニル酸シクラーゼ、一酸化窒素、機能性食品
配属学生
| 大学院生 | 0名 |
|---|---|
| 学部学生 | 6年次生:13名、5年次生:16名、4年次生:15名 |
所属教員
-
大喜多 守
教授 / 博士(薬学)
■担当科目
薬学入門(1年)、薬理・薬物治療学1A(2年)、薬理学4(3年)、薬理学実習(3年)、特別演習・実習(4~6年)、創薬薬理学(6年)
薬理学特論(大学院)、病態薬理学特論1・2(大学院)、薬効評価演習(大学院)
■所属学会および社会活動
日本薬学会、日本薬理学会(学術評議員)、日本循環薬理学会、日本NO学会、日本高血圧学会、日本心脈管作動物質学会(評議員) -
田和 正志
准教授 / 博士(医学)
■担当科目
機能形態学1(1年)、基礎薬理学(1年)、薬理学実習(3年)、特別演習・実習(4~6年)、アドバンスト薬理学(6年)
薬理学特論(大学院)、病態薬理学特論1・2(大学院)、薬効評価演習(大学院)
■所属学会および社会活動
日本薬理学会(学術評議員)、日本循環薬理学会、日本NO学会、日本高血圧学会、日本心脈管作動物質学会、日本薬学会
研究内容
(1)エンドセリン及び一酸化窒素の病態生理学的役割
エンドセリン(ET)は、我々の体が産生する物質としては最も強力な血管収縮性ペプチドであり、高血圧や心臓病などの発症に関わっていることが明らかにされています。一方、一酸化窒素(NO)は、血管内皮由来弛緩物質として見出され、その後の活発な研究から、血管系のみならず、心臓や神経系、内分泌臓器などにおいて広く分布し、重要な生理作用を発揮する事が明らかになっています。
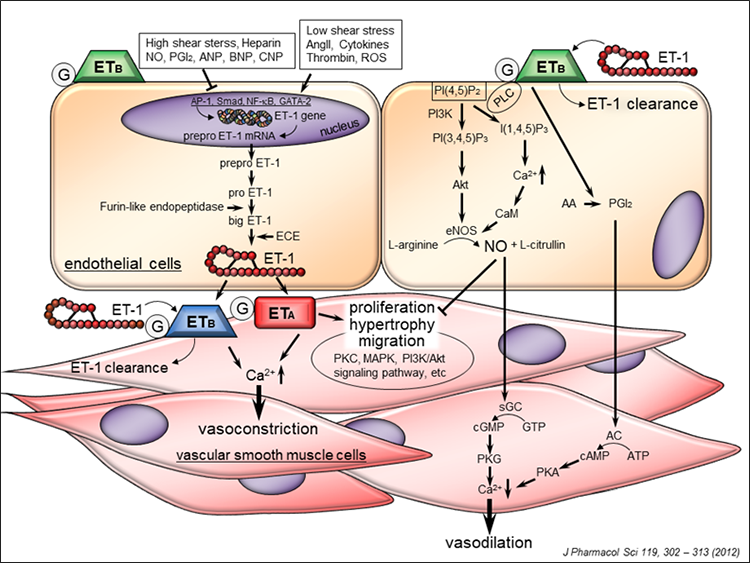
我々の研究室では、ETやNOの病態生理学的役割について幅広く検討しており、特に心臓や腎臓の交感神経調節機構、虚血再灌流障害における役割や、慢性的な腎障害の予防因子としての可能性についても検討しています。
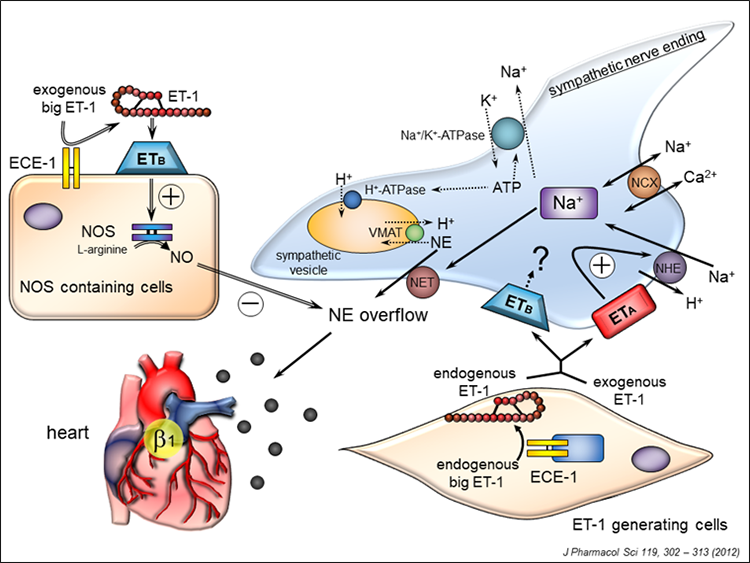


(2)急性腎障害に対する薬効評価およびメカニズム解析
急性腎障害(AKI)は確立された治療法がないことに加え、AKI発症後は慢性腎臓病(CKD)に移行し、最終的に末期腎不全に進行することが医療上大きな問題点として考えられています。我々の研究室では、AKIに対する治療薬ならびにAKI発症後の血管病変に着目し、CKDへの移行阻止の手段を検討しています。
(3)各種循環器疾患における可溶性グアニル酸シクラーゼの役割
可溶性グアニル酸シクラーゼ(sGC)は一酸化窒素(NO)の受容体としての役割を担っています。生体内においては、NOが活性化できるタイプ(還元型sGC)とできないタイプ(酸化型およびアポ型sGC)のsGCが存在しています。
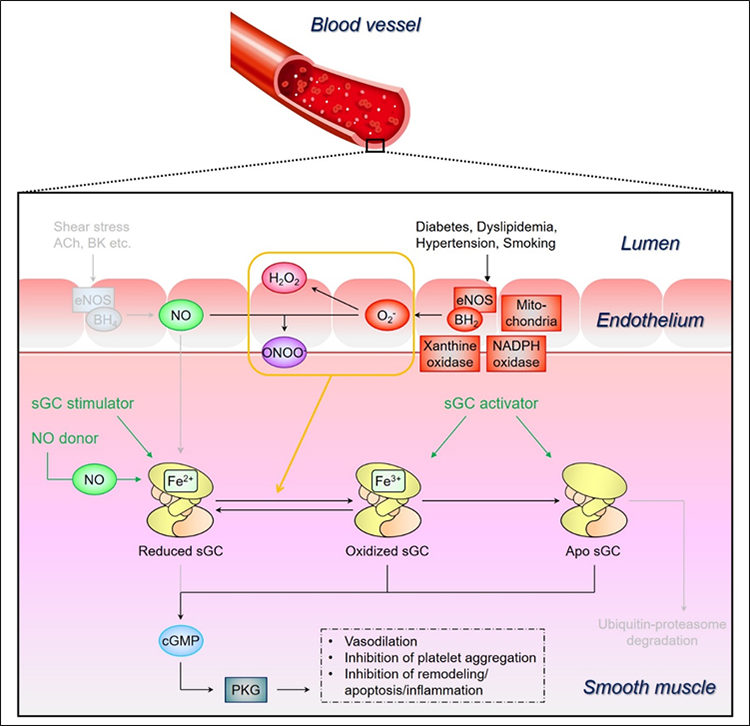
我々の研究室では、病態下においてsGCの酸化還元状態がどのように変化するのか、さらにはsGC刺激薬ならびにsGC活性化薬の治療効果も検証しています。

その他の研究
(4) 慢性腎臓病に対する予防ならびに治療薬の探索
(5) 機能性食品の循環器疾患(肺性高血圧など)予防効果とそのメカニズムの解明
参考論文
- 薬学雑誌 127, 1319-1329 (2007)
- Kidney Int. 73, 308-317 (2008)
- Circulation 111, 302-309 (2005)
- J. Pharmacol. Sci. 109, 7-13 (2009)
- J. Hypertens. 27, 92-101 (2009)
代表的論文
2025年
- Tawa M, Abe S, Fujita A, Ando R, Yoshinari H, Nakagawa K, Ohkita M. Beneficial effects of magnesium nitrate on disease severity in male rats with monocrotaline-induced pulmonary hypertension. Physiol Rep. 13(12):e70416, 2025.
- Nakagawa K, Oshiba Y, Sukita R, Hosomi A, Tawa M, Ohkita M. Roxadustat has beneficial effects on the vascular tone of the rat thoracic aorta. J Cardiovasc Pharmacol. 86(1):60-68, 2025.
- Tawa M, Nakagawa K, Ohkita M. Soluble guanylate cyclase stimulators and activators as potential antihypertensive drugs. Hypertens Res. 48(4):1458-1470, 2025.
- Tawa M, Nakagawa K, Ohkita M. Different sensitivities of porcine coronary arteries and veins to BAY 60-2770, a soluble guanylate cyclase activator. J Pharmacol Sci. 157(1):1-7, 2025.
2024年
- Tawa M, Nakagawa K, Ohkita M. Efficacy of BAY 60-2770, a Soluble Guanylate Cyclase Activator, for Coronary Spasm in Animal Models. J Pharmacol Exp Ther. 390(3):280-287, 2024
2023年
- Tawa M, Nakagawa K, Ohkita M. Effects of beetroot juice supplementation on vascular functional and structural changes in aged mice. Physiol Rep. 11(12):e15755, 2023
2022年
- Tawa M, Shimosato T, Nakagawa K, Okamura T, Ohkita M. Soluble Guanylate Cyclase-Mediated Relaxation in Aortas from Rats with Renovascular Hypertension. Pharmacology, 107(3-4):235-240, 2022
- Nakagawa K, Tanaka R, Donouchi M, Kanda M, Kamada S, Kobuchi S, Tawa M, Matsumura Y, Ohkita M. Vascular Endothelial Dysfunction in the Thoracic Aorta of Rats with Ischemic Acute Kidney Injury: Contribution of Indoxyl Sulfate. Oxid Med Cell Longev, 2022:7547269, 2022
- Nakagawa K, Kobayashi F, Kamei Y, Tawa M, Ohkita M. Acute Kynurenine Exposure of Rat Thoracic Aorta Induces Vascular Dysfunction via Superoxide Anion Production. Biol Pharm Bull, 45(4):522-527, 2022
- Tawa M, Okamura T. Factors influencing the soluble guanylate cyclase heme redox state in blood vessels. Vascul Pharmacol, 145:107023, 2022
2021年
- Nakagawa K, Itoya M, Takemoto N, Matsuura Y, Tawa M, Matsumura Y, Ohkita M. Indoxyl sulfate induces ROS production via the aryl hydrocarbon receptor-NADPH oxidase pathway and inactivates NO in vascular tissues. Life Sci. 265:118807, 2021
- Tawa M, Nagata R, Sumi Y, Nakagawa K, Sawano T, Ohkita M, Matsumura Y. Preventive effects of nitrate-rich beetroot juice supplementation on monocrotaline-induced pulmonary hypertension in rats. PLoS One, 16:e0249816, 2021
2020年
- Sato A, Nishioka S, Kiuchi Y, Imada K, Makino K, Nakagawa K, Tanaka R, Matsumura Y, Ohkita M Grape Extract from Chardonnay Seeds Restores Deoxycorticosterone Acetate-Salt-Induced Endothelial Dysfunction and Hypertension in Rats. Biol Pharm Bull. 43(1):59-67, 2020
2019年
- Kurumazuka D, Kitada K, Tanaka R, Mori T, Ohkita M, Takaoka M, Matsumurta Y α-Lipoic acid exerts a primary prevention for the cardiac dysfunction in aortocaval fistula-created rat hearts. Heliyon. e02371, 2019
- Ohkita M, Hayashi H, Ito K, Shigematsu N, Tanaka R, Tsutsui H, Matsumura Y Preventive Effects of Grape Extract on Ischemia/Reperfusion-Induced Acute Kidney Injury in Mice. Biol Pharm Bull. 42(11):1883-1890, 2019
- Koyama T, Tsubota A, Sawano T, Tawa M, Watanabe B, Hiratake J, Nakagawa K, Matsumura Y, Ohkita M Involvement of γ-Glutamyl Transpeptidase in Ischemia/Reperfusion-Induced Cardiac Dysfunction in Isolated Rat Hearts. Biol Pharm Bull. 42(11):1947-1952, 2019
- Feng YY, Tang M, Suzuki M, Gunasekara C, Anbe Y, Hiraoka Y, Liu J, Grasberger H, Ohkita M, Matsumura Y, Wang JY, Tsubata T. Essential Role of NADPH Oxidase-Dependent Production of Reactive Oxygen Species in Maintenance of Sustained B Cell Receptor Signaling and B Cell Proliferation. J Immunol. 202(9):2546-2557, 2019
2018年
- Tawa M, Furukawa T, Tongu H, Sugihara M, Taguwa S, Yamanaka M, Yano Y, Matsumori H, Kitada R, Sawano T, Tanaka R, Ohkita M, Matsumura Y Stimulation of nitric oxide-sensitive soluble guanylate cyclase in monocrotaline-induced pulmonary hypertensive rats. Life Sci., 203:203-209, 2018
- Tawa M, Yano Y, Yamanaka M, Sawano T, Iesaki K, Murata Y, Tanaka R, Nakagawa K, Ohkita M, Matsumura Y Effects of Beet Juice Supplementation on Monocrotaline-Induced Pulmonary Hypertension in Rats. Am J Hypertens.32(2): 216-222, 2019
2016年
- Tanaka R, Yazawa M, Morikawa Y, Tsutsui H, Ohkita M, Yukimura T, Matsumura Y:Sex differences in ischemia/reperfusion-induced acute kidney injury depends on the degradation of noradrenaline by monoamine oxidase. Clin. Exp. Pharmacol. Physiol.,44:371-377, 2016
2015年
- Kobuchi S, Tanaka R, Shintani T, Suzuki R, Tsutsui H, Ohkita M, Matsumura Y, Ayajiki K: Mechanisms underlying the renoprotective effect of GABA against ischaemia/reperfusion-induced renal injury in rats., Clin. Exp. Pharmacol. Physiol., 42:278-286, 2015
- Ueda K, Tsuji F, Hirata T, Ueda K, Murai M, Aono H, Takaoka M, Matsumura Y: Preventive Effect of SA13353, a Novel Transient Receptor Potential Vanilloid 1 Agonist, on Ischemia/Reperfusion-Induced Renal Injury in Rats., Advances in Pharmacology and Pharmacy.,3:30-42, 2015
2014年
- Kitada K, Yui N, Mori T, Ohkita M, Matsumura Y: Vasoprotective effects of an endothelin receptor antagonist in ovariectomized female rats., Life Sci., 118:379-385, 2014
- Kobuchi S, Tanaka R, Funai A, Suzuki R, Yazawa M, Tsutsui H, Ohkita M, Ayajiki K, Matsumura Y: Involvement of renal sympathetic nerve overactivation in the progression of chronic kidney disease in rats., J. Cardiovasc. Pharmacol., 63:9-15, 2014
- 田中亮輔, 松村靖夫: 急性腎障害(AKI)治療薬., 腎・高血圧の最新治療, 3:87-92, 2014
- 田中亮輔, 松村靖夫: 腎障害実験モデルの簡便な作製方法, 医薬品・医療機器の承認申請書の上手な書き方・まとめ方, 452-456, 2014
2013年
- Nishioka S, Yoshioka T, Nomura A, Kato R, Miyamura M, Okada Y, Ishizaka N, Matsumura Y, Hayashi T: Celiprolol reduces oxidative stress and attenuates left ventricular remodeling induced by hypoxic stress in mice., Hypertens. Res., 36:934-939, 2013
- Tsutsui H, Tanaka R, Yamagata M, Yukimura T, Ohkita M, Matsumura Y: Protective effect of ischemic preconditioning on ischemia/reperfusion-induced acute kidney injury through sympathetic nervous system in rats., Eur. J. Pharmacol., 718: 206-212, 2013
- Koyama T, Tawa M, Yamagishi N, Tsubota A, Sawano T, Ohkita M, Matsumura Y: Role of superoxide production in post-ischemic cardiac dysfunction and norepinephrine overflow in rat hearts., Eur. J. Pharmacol., 711:36-41, 2013
- Fukumoto T, Tawa M, Yamashita N, Ohkita M, Matsumura Y: Protective effects of 17beta-estradiol on post-ischemic cardiac dysfunction and norepinephrine overflow through the non-genomic estrogen receptor/nitric oxide-mediated pathway in the rat heart., Eur. J. Pharmacol., 699:74-80, 2013
- Kosaka S, Pelisch N, Rahman M, Nakano D, Hitomi H, Kobori H, Fukuoka N, Kobara H, Mori H, Masaki T, Cervenka L, Matsumura Y, Houchi H, Nishiyama A: Effects of angiotensin II AT1-receptor blockade on high fat diet-induced vascular oxidative stress and endothelial dysfunction in Dahl salt-sensitive rats., J. Pharmacol. Sci., 121:95-102, 2013
- 田中亮輔, 山本真也, 渡辺文太, 平竹潤, 大喜多守, 松村靖夫: 虚血性急性腎障害に対する新規選択的 γ-glutamyl transpeptidase 阻害薬 GGsTopTM の改善効果について, 腎とフリーラジカル, 11:146-149, 2013